摘要:通過對實驗室現有工業級聚合氯化鋁進行堿化度分析,向多個化學試劑廠調研得出,現場常用聚合氯化鋁的堿化度在1.5-2.7之間。通過合成不同堿化度(2.0-2.4)的聚合氯化鋁,對模擬成垢水進行系統的混凝實驗,考察堿化度對聚合氯化鋁混凝除硅的影響。
研究表明,堿化度會決定鋁形態的分布,進而影響混凝除硅的效果。隨著堿化度的升高,Ala含量逐漸降低,Alb含量先增加后減小,Alc含量逐漸增加。對模擬污水處理后,殘余硅酸形態有很大差異,用聚合氯化鋁(2.0)除硅后Sia含量變為32.1mg/L,Sic含量變為15.3mg/;聚合氯化鋁(2.2)除硅后Sia含量變為28.71mg/L,Sic含量變為30.5mg/L;聚合氯化鋁(2.4)除硅后Sia含量變為22.4mgL,Sic含量變為41.2mg/L。聚合氯化鋁(2.0) 除硅后Sia降低的比例較大,聚合氯化鋁(2.4)除硅后Sic降低的比例較大。隨著堿化度的升高,全硅剩余含量依次為47.4mg/L、59.5mg/L、63.6mg/L,表明堿化度越低,除硅效果越好。
聚合氯化鋁(PAC)是一種無機高分子混凝劑,分子式為[Al2(OH)nCl6-n]m(n為1-5,m≤10)。根據氫氧根離子的架橋作用和多價陰離子的聚合作用,生產分子量較大、電荷較高的無機高分子水處理藥劑,目前已大規模地應用于油田污水的混凝除硅。測定鋁形態常用的是Al-Ferron(高鐵試劑,7-碘-8-羥基哇琳-5-磺酸)逐時絡合比色法。對于溶液中硅的測定已有相當多的報道。采用臭氧把硅轉化為硅烷,用熒光法測量自然水中的硅含量。介紹了兩種直接、快速的堿分解和酸分解方法。采用電化學方法在原有的硅鉬黃光度法的機理基礎上進行了改進,提高了原方法的精度。在現場一般采用硅鉬黃光度法和硅鉬藍光度法。其中活性硅的測定一般采用HZ-HJ-SZ-0147,全硅的測定一般采用SS-6-2-84。
堿化度(Basicity,縮寫為B)是衡量聚合氯化鋁凈水效能的一個很重要的指標,通常將堿化度定義為聚合氯化鋁分子中[OH-]與[Al3+]的當量百分比([OH-]/[Al3+]×100%)。實踐表明,聚合氯化鋁的聚合度、電荷量、混凝效果、成品的pH值、使用時的稀釋率和儲存的穩定性等都與堿化度有密切關系,常用聚合氯化鋁的堿化度多為1.5-2.7。本文通過對遼河稠油污水水質的分析,實驗室配置模擬污水,制備了不同堿化度的聚合氯化鋁,考察硅、鋁在混凝除硅前后形態分布的變化,分析了堿化度對聚合氯化鋁除硅的影響。
1、實驗部分
1.1不同堿化度的聚合氯化鋁的制備
將氫氧化鈉、氯化鋁分別溶于水,在500mL的燒杯中加入少許水,加入1mL的濃鹽酸,加入氯化鋁,在80℃的恒溫水浴中,用SCM-L-Ⅱ型乳化機乳化(5000r/min),邊乳化邊向其中加入氫氧化鈉,控制滴加速率30min滴完,繼續乳化30min。冷卻后,將其定容到500mL的容量瓶中。
1.2結果分析
采用722型光柵分光光度計,分別在366nm、410nm處測量鋁、硅含量。
2、結果與討論
實驗室根據稠油污水水質分析,配置模擬成垢水,其中含有九水合硅酸鈉(SiO2)=473.39mg/L,[Ca2+]=26.15mg/L,[HCO3-]=1426.78mg/L,調pH值為8.31。
2.1硅酸形態的分析
2.1.1硅酸形態的測定
對硅鉬黃吸光度法測量活性硅的研究,可將硅酸區分為Sia、Sib、Sic。在硅酸與鉬酸的反應中,10min內能顯色的為Sia,被歸類為單體硅酸;10-30min能顯色的為Sib,被歸類為低聚體硅酸;30min內不與鉬酸反應的硅酸歸為Sic,被歸類為高聚體硅酸。自制模擬水中對硅形態測量如圖1所示。

對圖1進行分析得出,模擬水水中硅形態分布。將10min時的吸光度帶入標準曲線,所得硅含量為219.39mg/L,即為Sia的含量。將30min時所測定的吸光度帶入標準曲線中,所得硅含量為230.12mg/L,即為Sia和Sib的含量。用Sia和Sib的總含量減去Sia的含量,即為Sib的含量,為10.73mg/L。Sic的含量為全硅含量(473.39mg/L)減去Sia和Sib的總含量243.27mg/L。
2.1.2全硅(SiT)的測定
硅酸溶液與HF在沸水浴條件下30min內解離出的并能在10min內與鉬酸反應的硅酸即為全硅含量。參照標準SS-6-2-84,并對其作一定的優化,繪制的全硅法標準曲線,見圖2。
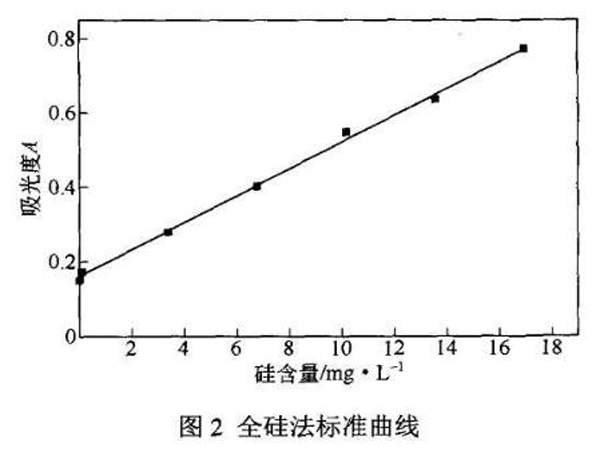
2.2鋁形態的分析
2.2.1鋁形態的測定
取適量水樣酸化后,加入Al-Ferron試劑顯色,分別于1min、120min時在波長366nm下測定其吸光度,與Al-Ferron標準曲線對照,測定試樣中的Al的形態。
利用Al-Ferron的顯色反應對鋁形態進行劃分。其原理是基于顯色劑Ferron與Al3+以及它的不穩定水解聚合形態發生解離絡合反應速率的差異,根據其逐時進展情況,將鋁溶液中的各種鋁形態相對區分為三類形態,即:單體形態Ala,是1min內與Ferron瞬時反應的部分;聚合形態Alb,是與Ferron緩慢反應的部分;溶膠或凝膠聚合物Al(OH)3,是與Ferron反應十分緩慢或基本不反應的部分。由圖中的1min的值可以直接計算出Ala的量, 120min的值可以計算出Ala和Alb的總值,再減去已知的Ala值即可求出Alb的量。Alc的值可以由通過EDTA滴定得到的總鋁濃度減去Ala和Alb的量得出。對某Al2O3含量為30%聚合氯化鋁分析曲線如圖3。

由圖3可見,1min讀出的吸光度值為0.27626,代入曲線得到Ala=0.00113×10-4mol/L;120min讀出的吸光度值為0.29048,代入曲線得到Ala+Alb=0.00202×10-4mol/L。Alb=0.00202-0.00113=0.00089×10-4mol/L,由EDTA滴定法得到AlT=0.004×10-4mol/L,則Alc=0.00198×10-4mol/L。因此,該聚合氯化鋁中Ala占28.25%,Alb占22.25%,Alc占49.5%。
2.2.2全鋁的測定
由于制備聚合氯化鋁的原料有可能含有可與乙二胺四乙酸(EDTA)絡合的其他金屬離子,以Ca2+離子較為顯著,本次試驗以EDTA為絡合劑,二甲酚橙為指示劑,用硝酸鉛置換滴定來降低其他金屬離子對滴定的干擾。滴定誤差為±5%。
2.3不同堿化度聚合氯化鋁的制備
對不同堿化度的考察,表1為實驗室自制堿化度為B=2.0,B=2.2和B=2.4的3種聚合氯化鋁的鋁形態分布。
表1不同堿化度聚合氯化鋁鋁形態分布
| 聚合氯化鋁 | 測得堿化度 | Ala/% | Alb/% | Alc/% |
| 聚合氯化鋁(2.0) | 2.00 | 33.4 | 34.7 | 31.9 |
| 聚合氯化鋁(2.2) | 2.20 | 18.6 | 45.1 | 36.3 |
| 聚合氯化鋁(2.4) | 2.39 | 9.3 | 33.5 | 57.2 |
由表1可以看出,聚合氯化鋁堿化度從2.0升到2.2時,Ala含量從33.4%變成18.6%,Alb含量從34.7%變為45.1%,Alc含量從31.9%變為36.3%,堿化度升到2.4時,Ala含量變為9.3%,Alb含量變為33.5%,Alc含量變為57.2%。 由此可見,隨著堿化度的升高,Ala含量逐漸降低,Alb含量先增加后減少,Alc含量逐漸增加。
2.4、聚合氯化鋁的除硅效果
用7天后聚合氯化鋁實驗,考察不同鋁分布的聚合氯化鋁的除硅效果。分別取一定量的聚合氯化鋁(2.0)、聚合氯化鋁(2.2)、 聚合氯化鋁(2.4)溶液,加入污水中使得總鋁含量為4×10-3mol/L,在70℃下反應,攪拌5min,靜置1h后,然后定容到500mL,離心,測定溶液中殘余的硅鋁形態。用Al-Ferron法在366nm下測定鋁形態,硅鉬黃光度法測Sia和Sic含量,HF轉換光度法測全硅含量,EDTA置換滴定法測全鋁含量,結果如圖4、圖5所示。


2.4.1除硅前后硅形態的變化
由圖4分析可知:Ala含量較高的聚合氯化鋁除硅后污水中Sic的含量更低,Alc含量高的聚合氯化鋁除硅后污水中Sia含量更低。針對相同硅形態的污水,采用不同鋁形態的聚合氯化鋁處理后,溶液中殘余的硅酸形態有很大差異,Sia與Sic的比例明顯不同。聚合氯化鋁(2.0)除硅后Sia降低的比例較大,聚合氯化鋁(2.4)除硅后Sic降低的比例較大。
2.4.2除硅前后鋁形態的變化
由圖5可見,聚合氯化鋁(2.0)反應前Ala、Alb、Alc的比例接近于1:1:1,反應后比例變為2:1:1;聚合氯化鋁(2.2)反應前Ala、Alb、Alc的比例接近于1:3:3,反應后比例變為1:2:1;聚合氯化鋁(2.4)反應前Ala、Alb、Alc的比例接近于1:6:12,反應后比例變為1:2:3。
3、結論
(1)制備不同堿化度的聚合氯化鋁,其Ala、Alb、Alc含量差別很大,堿化度較低的聚合氯化鋁中Ala比例更高,中等堿化度的聚合氯化鋁中Alb含量高,高堿化度時Alc含量更高。制備后各聚合氯化鋁溶液中的各類鋁形態還會發生緩慢的相互轉換,在4天后基本達到平衡。
(2)Ala含量較高的聚合氯化鋁除硅后污水中Sic的含量更低,Alc含量高的聚合氯化鋁除硅后污水中Sia含量更低。這表明聚合氯化鋁的除硅效果可能是通過其在水中的各類水解形態間的協同作用來實現的。
(3)綜合考察3種不同堿化度的聚合氯化鋁的形態及其除硅效果,反應前后對比發現,隨著堿化度的升高,Sia的降低幅度逐漸增加,Sic的降低幅度逐漸減小,從全硅來看,在本文研究范圍內,堿化度越高,除硅效果越差。

